关于医疗器械出产草创企业而言,产品从研制规划阶段到走向消费市场,至少应阅历规划开发、注册检测、临床试验、注册申报、出产答应请求等绵长的无盈余进程。那么,怎么评价产品安全性危险、申报注册周期、投入资金与本钱?都是草创企业创始人最关怀的问题。根据以上问题,小编进行依照产品规划开发、系统树立、立异产品申报(若触及)、注册检测、临床试验、注册申报、出产答应请求、产品上市等必要阶段进行简略收拾。
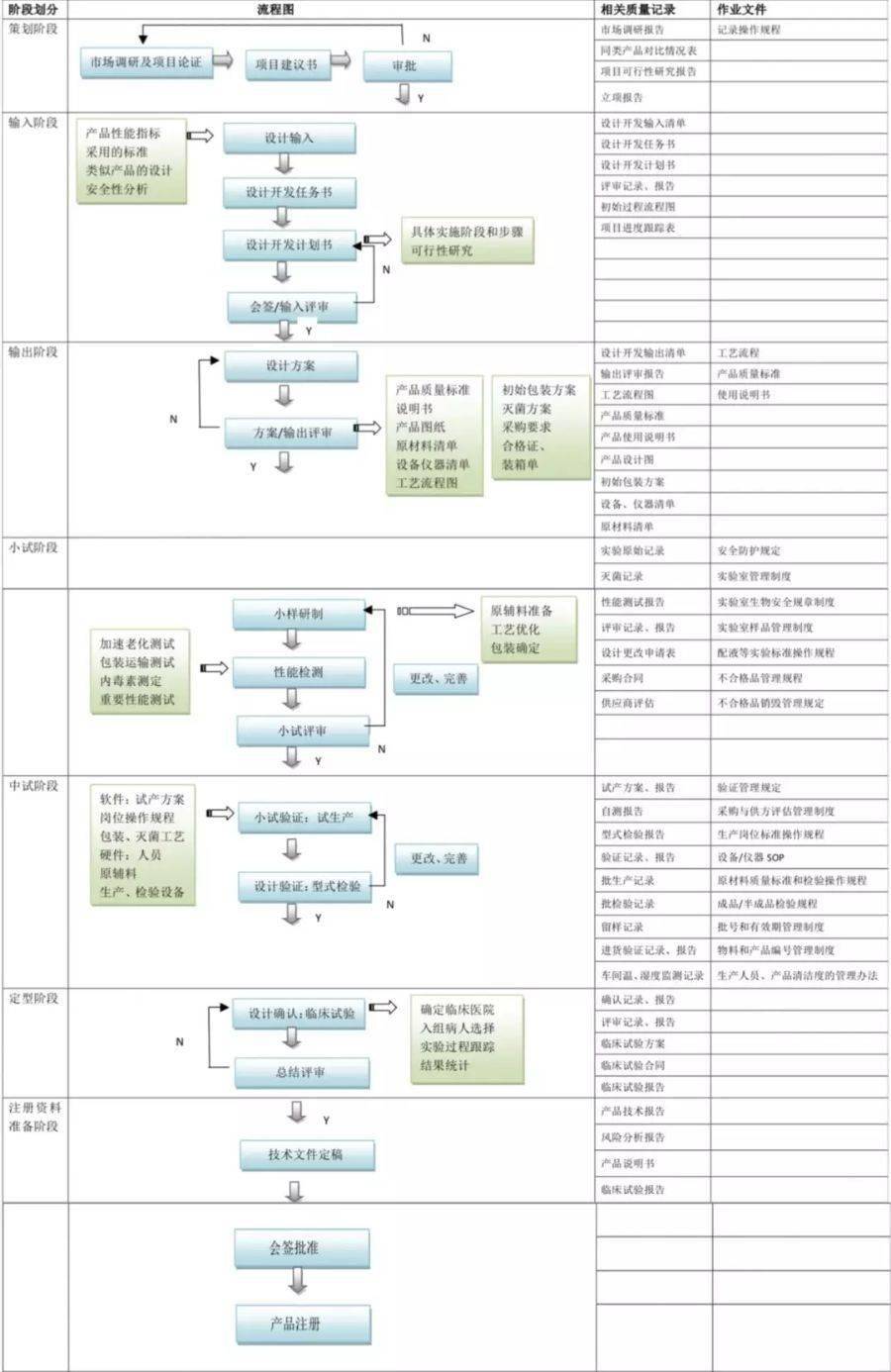
产品规划开发可分7个阶段:策划阶段、规划输入阶段、规划输出阶段、小试阶段、中试阶段、定型阶段、注册材料预备阶段。
一般来说,创始人创建公司是根据科研成果与产品布局根底上,并已开端具有研制团队、合作伙伴等。但无论怎么,关于草创公司而言,因触及许多资金注入与技能攻坚,产品规划开发阶段十分困难,时刻也是难以预估的,短则数月,长则数年。那么,怎么在产品规划开发阶段削减相关本钱,满意需求,添加立异?
首要,产品技能层面,专业高效的开发团队是条件和根底;其次,法规层面主张寻觅专业研制服务企业或引入法规团队对产品研讨开发进行严厉的危险评价,清晰产品申报类型等。但咱们常常发现,许多新办企业在产品已定型、开模后,才开端引入法规人员或寻觅咨询机构。此刻的主张和办法往往根据弥补,严峻的或许触及改模、从头规划等。所以关于新办企业而言,法规前置应稳重考量。最终,还应重视产品专利布局。公司应要点布局中心技能的知识产权维护;一起,考虑中心技能转让、购买等问题。
2014年2月7日,原国家食药监总局发布了《立异医疗器械特别批阅程序(试行)》(食药监械管〔2014〕13号),此文件自2014年3月1日起实施。该程序是在保证上市产品安全、有用的条件下,针对立异医疗器械设置的批阅通道,但也有苛刻的批阅规范:(1)产品中心技能创造专利权,批阅请求人经过其技能立异活动,在我国依法具有产品中心技能创造专利权,或许依法经过受让获得在我国创造专利权或其使用权,或许中心技能创造专利的请求已由国务院专利行政部门揭露;(2)国内首创产品,首要作业原理/效果机理为国内首创,产品功能或许安全性与同种类型的产品比较有根本性改善,技能上处于世界领先水平,而且具有十分显着的临床使用价值;(3)产品根本定型,请求人已完结产品的前期研讨并具有根本定型产品,研讨进程实在和受控,研讨数据完好和可溯源。
若企业产品规划满意上述要求,则应着手申报立异。立异特别批阅是请求人已完结产品的前期动物研讨并具有根本定型产品即可申报。申报流程详见图2。



